Brechungsindexdetektion in der HPLC verstehen – Unsichtbares sichtbar machen
Wenn es um HPLC-Detektoren geht, stehen UV/VIS-Systeme meist im Rampenlicht, und das aus gutem Grund. Sie sind empfindlich, selektiv und vielseitig einsetzbar. Doch was ist, wenn dein Analyt im UV- oder sichtbaren Bereich keine Absorption aufweist?
Hier kommt der Brechungsindex-Detektor (engl. Refractive Index Detector, RID) ins Spiel. Unauffällig, zuverlässig, erstaunlich vielseitig und oft als „Universaldetektor“ der HPLC bezeichnet, macht er Verbindungen sichtbar, die für andere Detektoren unsichtbar bleiben. Wenn du Verbindungen wie Zucker, Polymere, Lipide oder Alkohole analysierst, hast du wahrscheinlich schon einmal einen solchen Detektor verwendet oder dich gefragt, ob du das tun solltest.
Werfen wir einen genaueren Blick darauf, wie die RI-Detektion funktioniert, wo ihre Stärken liegen und wie man die beste Leistung aus ihr herausholt.
💡Funktionsweise der RI-Detektion
Wenn Licht von einem Medium in ein anderes übergeht, wird es je nach Phasengeschwindigkeit und Einfallswinkel abgelenkt (oder gebrochen). Dieses Verhalten wird durch das Snelliussches Brechungsgesetz beschrieben, das besagt, dass der Brechungsgrad durch den Brechungsindex (engl. refractive index, RI) des Mediums bestimmt wird (siehe Abbildung 1).
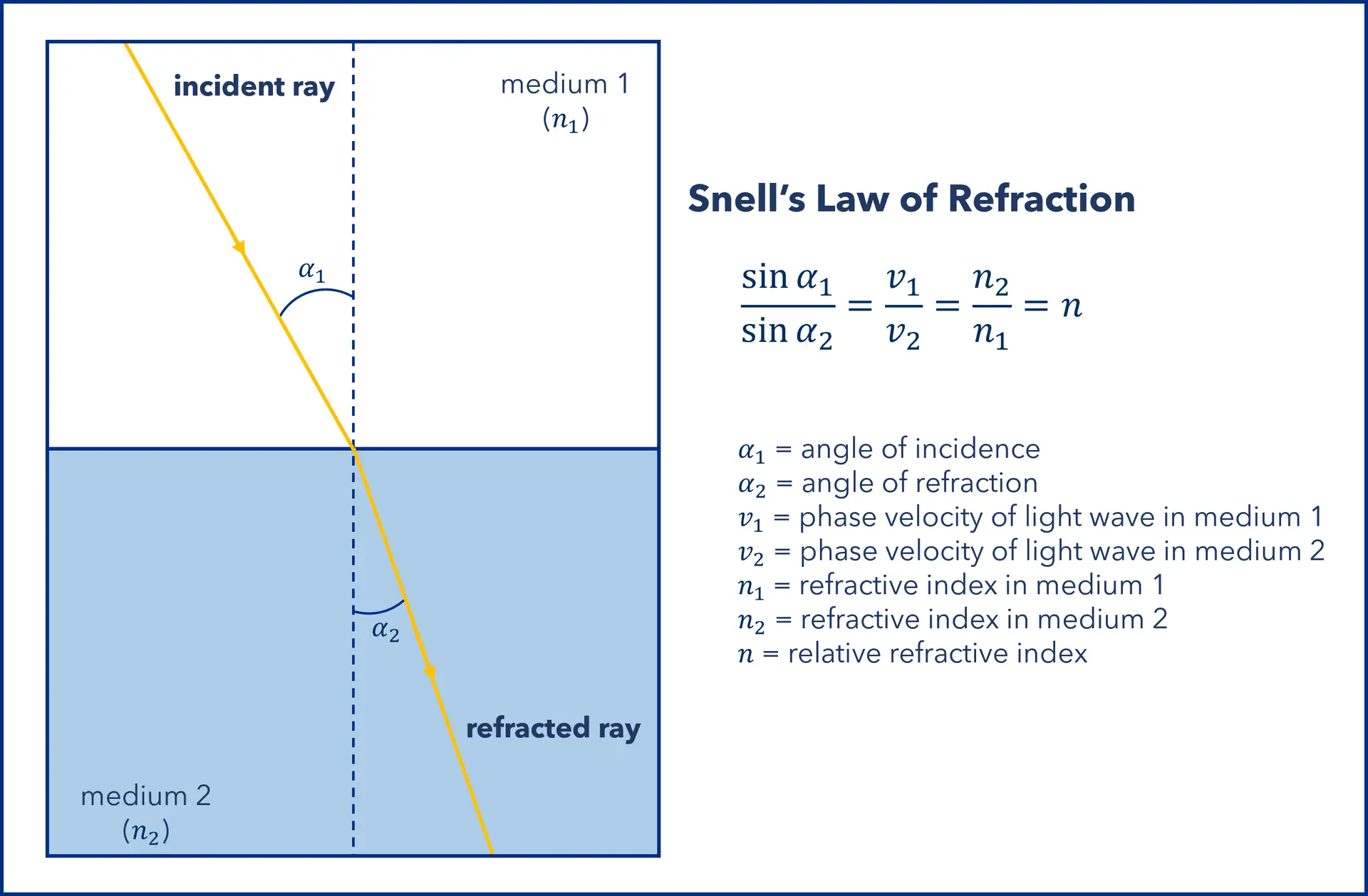
Abbildung 1: Brechung von Licht an einer Grenzfläche zwischen zwei Medien mit unterschiedlichen Brechungsindizes, wobei n₁ > n₂ ist. Da die Lichtgeschwindigkeit im zweiten Medium geringer ist (v₂ < v₁), ist der Brechungswinkel α₂ kleiner als der Einfallswinkel α₁. (Grafik von KNAUER)
In der HPLC misst ein RI-Detektor kleinste Unterschiede im Brechungsindex der mobilen Phase, während ein Analyt aus der Säule eluiert. Da jede Substanz ihren eigenen Brechungsindex hat, lassen sich selbst minimale Veränderungen in der Zusammensetzung des Eluenten nachweisen.
Moderne RI-Detektoren arbeiten nach dem Differentialprinzip (siehe Abbildung 2) und vergleichen kontinuierlich zwei Lichtwege: einen, der durch eine Referenzzelle mit reiner mobiler Phase verläuft, und einen, der durch eine Probenzelle mit Eluat (mobile Phase + Analyt) verläuft. Ein Lichtstrahl, meist von einer LED oder einer Wolframlampe, durchläuft beide Zellen. Eine Photodiode misst jede Abweichung im Lichtweg, sobald es Unterschiede im Brechungsindex gibt.
Wenn nur die mobile Phase fließt, sind beide Strahlengänge optisch identisch. Der Lichtstrahl durchläuft die Zelle ohne Ablenkung, und es wird kein Signal erfasst. Wenn ein Analyt eluiert, verändert er den Brechungsindex in der Probenzelle, wodurch der Strahl leicht abgelenkt wird und ein optisches Ungleichgewicht entsteht. Diese Verschiebung führt zu einer Änderung der Lichtintensität, die erfasst und in ein elektrisches Signal umgewandelt wird, das im Chromatogramm als Peak erscheint. Das Signal ist proportional zur Analytkonzentration, was eine quantitative Analyse ermöglicht.
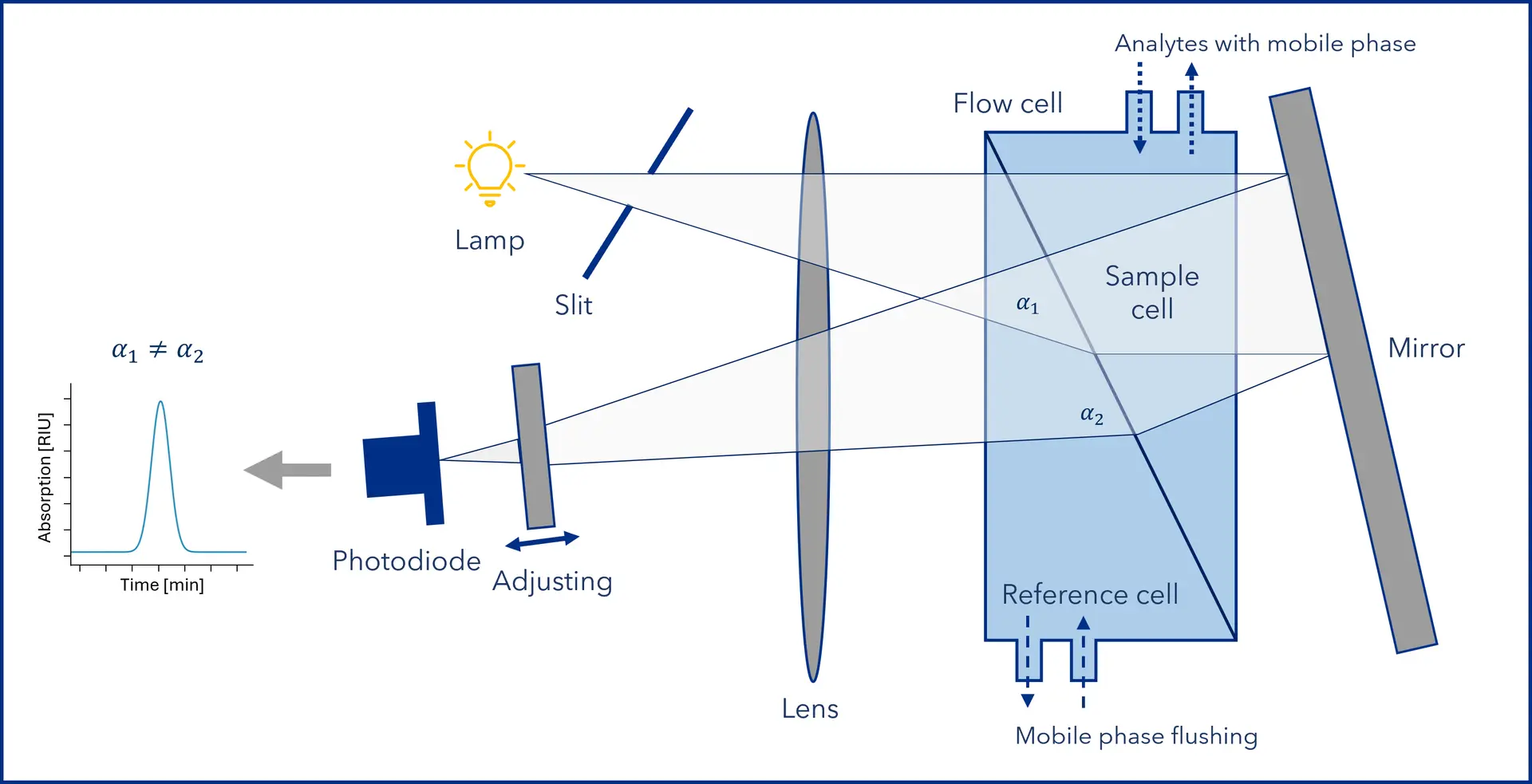
Abbildung 2: Schematische Darstellung eines Differential-RI-Detektors mit dualer Flusszelle. Die Probenzelle enthält das Säuleneluat, die Referenzzelle reine mobile Phase. Ein Lichtstrahl durchläuft beide Zellen und erzeugt ein Spaltbild auf einer Photodiode. Jede durch den Analyten verursachte Änderung des Brechungsindexes verändert den Strahlengang, verschiebt das Bild auf der Photodiode und erzeugt so einen Signalpeak. (Grafik von KNAUER)
Um stabile Messergebnisse zu gewährleisten, muss die Referenzzelle stets mit derselben mobilen Phase befüllt sein wie die Probenzelle (ohne Analyt); daher wird sie regelmäßig mit frischer mobiler Phase gespült, in der Regel über ein Umschaltventil und/oder ein T-Stück (siehe Abbildung 3).
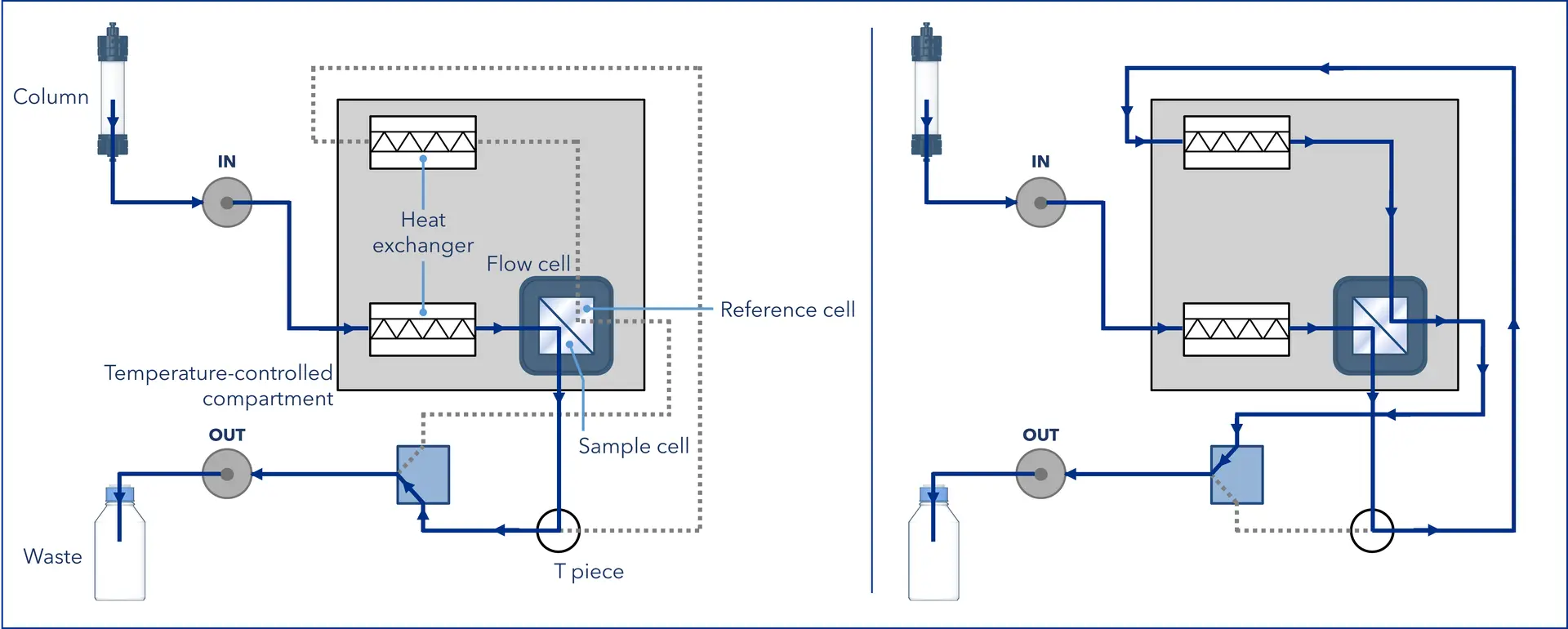
Abbildung 3: Flussweg im AZURA® RID 2.1L während der Analyse (links) und des Spülvorgangs (rechts). Während der Analyse fließt das Lösungsmittel vom IN-Anschluss durch den Wärmetauscher und die Probenzelle und dann weiter durch das T-Stück und das Spülventil zum OUT-Anschluss. Während des Spülvorganges leitet das Ventil den Fluss durch das T-Stück um, sodass das Lösungsmittel einen zweiten Wärmetauscher und die Referenzzelle passiert, bevor es über den OUT-Anschluss austritt. (Grafik von KNAUER)
Es ist wichtig zu wissen, dass der Brechungsindex sowohl von der Lichtwellenlänge als auch von der Dichte des Mediums abhängt. Während die Wellenlänge durch die Konstruktion des Detektors festgelegt ist, variieren die Dichte und damit der Brechungsindex in Abhängigkeit von Temperatur, Druck und Zusammensetzung des Mediums. Das führt dazu, dass die Brechungsindex-Detektion sehr empfindlich auf Schwankungen der Betriebsbedingungen reagiert. Wir werden dieses Thema in den nächsten Abschnitten näher beleuchten.
💡Warum der RID überzeugt: Die großen Vorteile
RI-Detektoren spielen ihre Stärken besonders dann aus, wenn andere Detektionsmodi nicht mehr weiterwissen. Sie sind vielleicht nicht die auffälligste Option, bieten jedoch entscheidende Vorteile, die sie für bestimmte Analyten unverzichtbar machen.
🌍 Universelle Detektion
RIDs erkennen jeden Analyten, der den Brechungsindex der mobilen Phase verändert – ganz ohne Chromophore. Und da so gut wie alles den Brechungsindex beeinflusst, wird die RI-Detektion als „universeller Detektor“ bezeichnet. Das heißt, wir können zuverlässig Zucker, Alkohole, Lipide, Fettsäuren oder Polymere erkennen.
♻️ Nicht-destruktiv
Bei der RI-Detektion bleibt deine Probe unversehrt, perfekt für präparative HPLC oder wenn Proben weiterverwendet werden sollen. Entdecke hier den AZURA® RID 2.1L von KNAUER für präparative Anwendungen bis zu 100 ml.
⚙️ Einfach & Zuverlässig
RI-Detektoren eignen sich super für wässrige und viele organische mobile Phasen, solange deren Zusammensetzung gleich bleibt (Hallo, isokratische Läufe 👋). Unter stabilen Bedingungen brauchen sie kaum Wartung, sind robust und einfach zu bedienen.
🧪 Direkte Messung
Bei der RI-Detektion sind keine chemische Derivatisierung oder Markierung erforderlich, um Analyten „sichtbar“ zu machen. Solange sie in der mobilen Phase löslich sind und den Brechungsindex beeinflussen, können sie nachgewiesen werden. Das vereinfacht die Probenvorbereitung und reduziert potenzielle Fehler.
Dank dieser Einfachheit eignet sich die RI-Detektion hervorragend für Routineanalysen wie die Quantifizierung von Laktose in Milch oder die Überprüfung der Reinheit von Polymeren.
💡Die Herausforderungen: Wo der RID „zickig“ wird
Jeder Detektor hat seine Eigenheiten, und RI-Detektoren sind da keine Ausnahme. Sie sind wunderbar universell, aber um ihre beste Leistung zu bringen, brauchen sie stabile und gut kontrollierte Bedingungen. Ein bisschen „Diva“ steckt also in ihnen drin. 😉
Hier sind die wichtigsten Herausforderungen.
🌡️ Temperaturempfindlichkeit
RI-Detektoren reagieren äußerst empfindlich auf Temperaturänderungen. Der Brechungsindex n variiert linear mit der Temperatur (dn/dT ≈ 10⁻⁴/°C bei wässrigen Lösungsmitteln), sodass selbst kleinste Schwankungen zu einer merklichen Basislinienverschiebung führen können, die die Signale der Analyten übersteigt.
Deshalb sind RI-Detektoren mit thermostatisierten Kammern und Wärmetauschern ausgestattet, um die Temperatur der Flusszelle zu stabilisieren. Dies ermöglicht eine genaue und reproduzierbare Detektion. Aber die Wärmetauscher verursachen auch ein zusätzliches Totvolumen, was die Peaks im Vergleich zur UV-Detektion verbreitern kann.
⚗️ Keine Gradienten möglich
RI-Detektion funktioniert praktisch nur isokratisch. Jede Änderung der Zusammensetzung der mobilen Phase verursacht größere RI-Änderungen als der Analyt selbst. Das führt zu Basislinienverschiebungen, die Peaks verdecken können. Damit die Basislinie stabil bleibt, müssen die Proben- und Referenzzellen während des gesamten Laufs dieselbe mobile Phase enthalten.
🔍 Geringe Empfindlichkeit
Im Vergleich zu UV ist die RI-Detektion weniger empfindlich, in der Regel um 1-2 Größenordnungen schlechter. Nachweisgrenzen liegen meist im µg-mg/mL-Bereich, weshalb sich diese Methode weniger gut für Spurenanalysen oder die Bestimmung von Verunreinigungen eignet.
💪 Druckempfindlichkeit
RI-Flusszellen vertragen nur einen begrenzten Rückdruck. Daher muss der RI-Detektor bei Reihenschaltung immer als letzter Detektor im System angeordnet werden.
⏱️ Lange Equilibrierungszeit
RI-Detektoren benötigen Zeit, um sich zu stabilisieren. Das Aufwärmen und Equilibrieren können mehrere Stunden dauern, bis eine konstante Basislinie erreicht ist.
📉 Empfindlichkeit der Basislinie
Die RI-Detektion reagiert auf jede Änderung des Brechungsindex. Selbst bei konstanter Temperatur können Fluss- und Druckschwankungen, Luftblasen, Pumpenpulsationen, eine unzureichende Durchmischung des Laufmittels oder Verunreinigungen in der mobilen Phase zu Rauschen oder Drift führen.
Daher ist ein sauberer und stabiler Betrieb unerlässlich.
💡Tipps für optimale RI-Detektion
Der Schlüssel zum effektiven Einsatz eines RI-Detektors lautet: Stabilität. Schon kleinste Änderungen der Betriebsbedingungen können sich schnell in der Basislinie bemerkbar machen und die Datenqualität beeinträchtigen. Daher lohnt es sich, bei der Einrichtung und Handhabung des RID etwas Sorgfalt walten zu lassen.
🌡️ Temperatur konstant halten
Die thermische Stabilität ist in der Regel das A und O. Der Detektor, die Säule und die mobile Phase sollten vor Beginn eines Laufs mindestens 60 Minuten lang vollständig equilibrieren. Verwende am besten einen Säulenofen und halte Detektor und Säule nach Möglichkeit auf derselben Temperatur. Versuche, Umgebungseinflüsse so gering wie möglich zu halten, denn Zugluft, Sonnenlicht oder Temperaturschwankungen im Labor zwischen Tag und Nacht können die Ergebnisse beeinträchtigen.
📈 Isokratisch arbeiten
RI-Detektoren erfordern eine gleichbleibende Zusammensetzung der mobilen Phase; halten dich also an isokratische Methoden. Wenn die Methode auf Gradienten basiert, ist dieser Detektor einfach nicht das richtige Werkzeug.
🫧 Entgasen & Sauber arbeiten
Verwende nur vollständig entgaste, partikelfreie mobile Phasen und stelle sicher, dass das System ordnungsgemäß entlüftet ist. Nutze den Inline-Entgaser des LC-Systems. Halte Schläuche, Lösungsmittel und den Flussweg sauber. Winzige Luftblasen und Verunreinigungen können Spikes, Rauschen oder falsche Signale verursachen.
🧪 Proben richtig vorbereiten
Proben sollten in der mobilen Phase oder in einem Lösungsmittel, das dieser sehr ähnlich ist, gelöst werden, um RI-Sprünge während der Totzeit zu vermeiden. Außerdem sollten die Proben immer gefiltert werden, um das Risiko einer Verstopfung zu verringern und die Durchflusszelle zu schützen.
💪 Fluss & Druck stabilisieren
Halte die Durchflussraten konstant und vermeide plötzliche Druckschwankungen, übermäßige Pumpenpulsationen und Leckagen. Eine kleine Restriktionskapillare oder ein Rückdruckregler, die hinter der Zelle installiert sind, können zur Druckstabilisierung beitragen. Sie beheben jedoch kein Rauschen, das durch Probleme mit der Pumpe entsteht.
⚙️ Wartung, Auswertung & praktische Hinweise
Spüle die Referenzzelle täglich mit frischer mobiler Phase und wechsle die mobile Phase regelmäßig aus, um mikrobielles Wachstum oder Zusammensetzungsänderungen durch Verdunstung zu verhindern. On-line Mischen der mobilen Phasen sollte nach Möglichkeit vermieden werden.
Wenn das Lösungsmittelsystem gewechselt wird, muss der Detektor mit untereinander mischbaren Lösungsmitteln gespült werden. Plane ausreichend Zeit für das Re-Equilibrieren ein. Die Verwendung eines Recycle-Modus für die mobile Phase oder das Versetzen des Detektors in einen Standby-Modus bei geringem Fluss zwischen den Läufen kann dazu beitragen, Lösungsmittel zu sparen und die Wiederanlaufzeit zu verkürzen.
👉 Pro-Tipp: Beobachte die Basislinie genau, eine stabile Basislinie ist das beste Zeichen dafür, dass das System ordnungsgemäß equilibriert ist. Und: Negative Peaks sind völlig normal; sie bedeuten nur, dass der Analyt einen niedrigeren Brechungsindex als die mobile Phase hat, und sind nicht unbedingt ein Systemfehler.
🎯 Fazit
Mit Fokus auf diese Details, liefert ein RI-Detektor stabile Basislinien sowie zuverlässige und reproduzierbare Quantifizierung. Halte das System sauber, die Temperatur konstant und die mobile Phase gleichbleibend – dann wird die „Diva“ zum Star.😉
💡Typische Anwendungen: Wo die RI-Detektion glänzt
Die RI-Detektion spielt ihre Stärken besonders dann aus, wenn die Analyten kein UV-Licht absorbieren. Daher ist sie perfekt für Verbindungen ohne starke Chromophore, wie beispielsweise Zucker, Alkohole, Fettsäuren, Polymere, Lipide und andere kleine organische Moleküle.
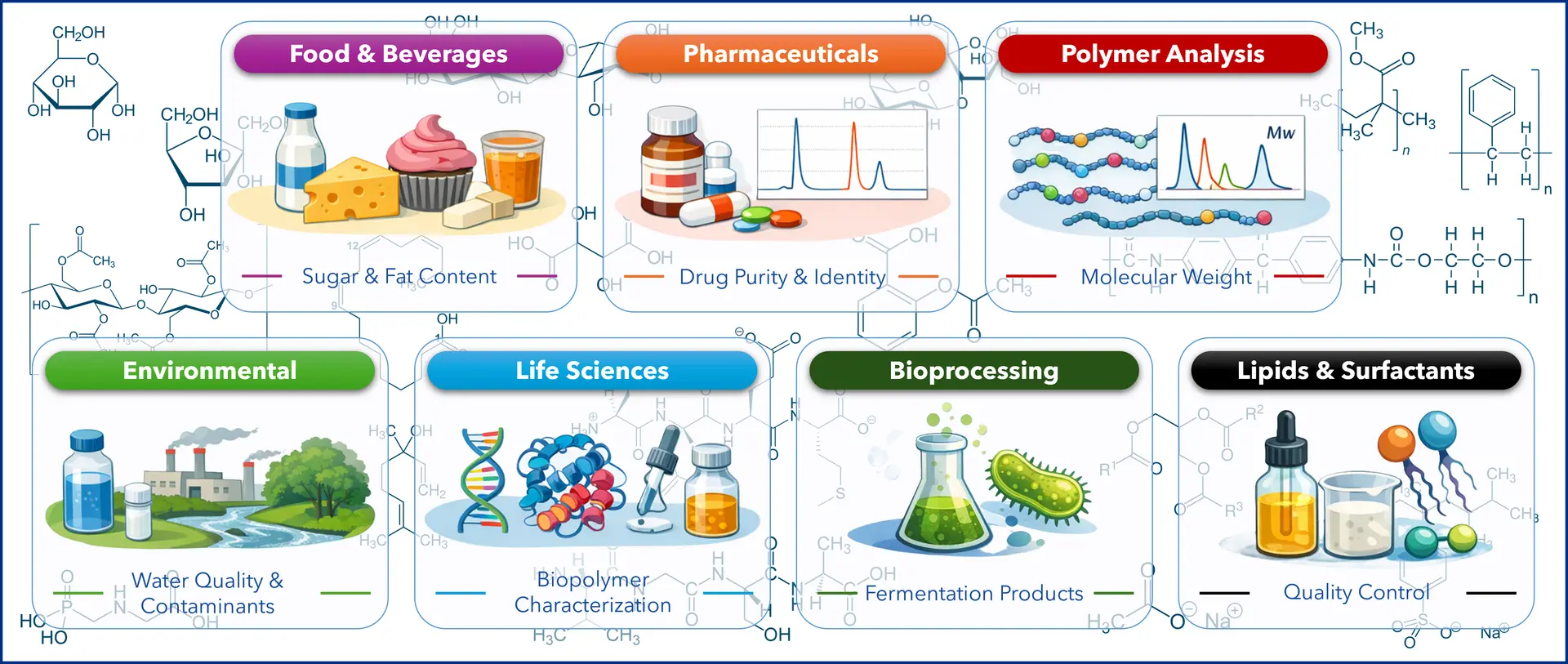
Abbildung 4: Gängige Anwendungsbereiche der RI-Detektion in der HPLC. (Grafik von KNAUER. Symbole erstellt mit DALL-E 3, OpenAI, GPT-5.4; 10. April 2026)
Zu den typischen Anwendungsbereichen gehören:
Kohlenhydrat- und Zuckeranalyse, z. B. zur Bestimmung von Glukose, Fruktose, Saccharose oder Laktose in Lebensmitteln und Getränken. Unsere Kollegin Julia hat kürzlich die HPLC-RI zur Qualitätskontrolle von Gummibärchen eingesetzt. Schaut euch gerne auch einmal ihren Blogbeitrag zu diesem Thema an. Aber Vorsicht, beim Lesen könnte euch das Wasser im Mund zusammenlaufen 😉. Außerdem hat sie den Brechungsindexdetektor AZURA® RID 2.1L von KNAUER genutzt, um gleichzeitig Zucker und organische Säuren in Wein zu bestimmen, und enthüllte so „The hidden science in your glass“.
Charakterisierung von Polymeren und Makromolekülen in GPC/SEC-Workflows, wie z. B. die Bestimmung der Molekulargewichtsverteilung. Erfahre hier, wie die Molekulargewichtsbestimmung mit einem KNAUER AZURA® GPC/SEC-System optimiert werden kann oder wie Mucinproteine mit einem AZURA® SEC-System analysiert werden können.
Bioprocessing, z. B. die Überwachung von Fermentationsprodukten wie Fruktane.
Pharmazeutische Anwendungen, z. B. die Analyse von Hilfsstoffen wie Zuckern oder Polyolen oder die Überprüfung der Identität und Reinheit von Wirkstoffen. Dextrane, die als Trägersubstanz in Arzneimitteln und als Verdickungsmittel und Feuchtigkeitsspender in Kosmetika verwendet werden, werden mittels SEC charakterisiert, da ihre spezifischen Eigenschaften von einer bestimmten Molekulargewichtsverteilung abhängen.
Lipid- und Tensidanalyse für die Qualitätskontrolle und Formulierungsarbeit.
Umweltanalytik, z. B. Nachweis organischer und anorganischer Verunreinigungen in Wasserproben.
Kurz gesagt: Die RI-Detektion funktioniert am besten, wenn die Analyten löslich und in Lösung stabil sind und unter einfachen isokratischen Bedingungen analysiert werden können. Sie ist zwar nicht für Spurenanalysen, Gradientenmethoden oder MS-gekoppelte Arbeitsabläufe geeignet, aber sie ist eine zuverlässige und praktische Lösung für Verbindungen, die mit UV- oder Fluoreszenzdetektion nur schwer nachzuweisen sind.
💡Fazit: Ein unterschätzter Klassiker
In einer Welt immer fortschrittlicherer Detektionstechnologien wirkt die RI-Detektion vielleicht unspektakulär, aber sie ist extrem zuverlässig. Für Verbindungen wie Zucker, Alkohole und Polymere bietet sie eine einfache, zuverlässige und nicht-destruktive Möglichkeit, das zu erkennen, was andere Methoden möglicherweise übersehen.
Ihre Grenzen liegen vor allem in der Temperaturempfindlichkeit und der fehlenden Gradiententauglichkeit. Am besten funktioniert sie also mit sorgfältig kontrollierten isokratischen Methoden. In der richtigen Konfiguration bleibt die RI-Detektion jedoch ein praktisches Arbeitstier im Labor – was beweist, dass manchmal Einfachheit und Universalität genau das sind, was man braucht.
Merke: Wenn dein Analyt „unsichtbar“ zu sein scheint, brauchst du vielleicht nur eine andere Perspektive. Die RI-Detektion könnte das perfekte Werkzeug sein, um ihn sichtbar zu machen.
Entdecke hier die Brechungsindex-Detektoren von KNAUER oder kontaktiere unser Vertriebsteam, um Hilfe bei der Auswahl des richtigen Detektors für deine Anforderungen zu erhalten
Im nächsten Beitrag unserer Blogserie „Sehen heißt Verstehen – Detektion leicht gemacht“ widmen wir uns der Fluoreszenzdetektion (FLD), einer hochselektiven und äußert empfindlichen Methode für Verbindungen, die fluoreszieren oder dazu gebracht werden können.
Für weitere Informationen zu diesem Thema kontaktiere bitte unsere Autorin: huhmann@knauer.net
Literatur
L. R. Snyder, J. J. Kirkland, J. W. Dolan, Introduction to Modern Liquid Chromatography, 3rd Edition, John Wiley & Sons, Inc., Hoboken, New Jersey, 2010.
D. A. Skoog, F. J. Holler, S. R. Crouch, Principles of Instrumental Analysis, 7th Edition, Cengage Learning, Boston, 2018.
R. P. W. Scott, Liquid Chromatography Detectors. In J. Chromatogr. Library, Vol. 11, Elsevier Scientific Publishing Company, Amsterdam, 1977, pp. iii-ix, 1-248.
V. R. Meyer, Praxis der Hochleistungs-Flüssigchromatographie, 10., vollst. überarb. u. erw. Auflage, Wiley-VCH, Weinheim, 2009.
G. Aced, H. J. Möckel, Liquidchromatographie, Apparative, theoretische und methodische Grundlagen der HPLC, VCH Verlagsgesellschaft mbH, Weinheim, 1991.
M. W. Dong, HPLC and UHPLC for Practicing Scientists, 2nd Edition, John Wiley & Sons, Inc., Hoboken, New Jersey, 2019.

