Überblick über HPLC-Detektionstechniken – Leistungsparameter von LC-Detektoren
Im letzten Blogbeitrag haben wir einen Überblick über die verschiedenen Typen von HPLC-Detektoren gegeben. In diesem Artikel werfen wir einen genaueren Blick auf die Leistungsparameter von LC-Detektoren und diskutieren Kriterien und Spezifikationen, die bei der Bewertung ihrer Eignung für bestimmte chromatographische Trennungen berücksichtigt werden sollten. Darüber hinaus vergleichen wir verschiedene Detektortypen und geben praxisnahe Hinweise zur Auswahl der passenden Detektionstechnologie.
Was macht einen idealen HPLC-Detektor aus?
Angesichts der Vielzahl an verfügbaren HPLC-Detektoren stellt sich schnell die Frage: Warum gibt es keinen einzigen Detektor, der für alle Anwendungen geeignet ist? Die einfache Antwort: Kein Detektor kann alle analytischen Anforderungen gleichzeitig erfüllen. Dennoch orientieren sich die meisten Detektorkonzepte an einer gemeinsamen Reihe idealer Eigenschaften.

Abbildung 1: Anforderungen an Detektoren. (Grafik von KNAUER)
1. Hohe Empfindlichkeit – Kleinste Signale sicher erfassen
Ein idealer Detektor sollte in der Lage sein, sehr geringe Substanzmengen im Nano- oder Pikogrammbereich zu „sehen“. Eine hohe Empfindlichkeit verbessert die Nachweisgrenze (engl. Limit of detection, LOD), reduziert den Aufwand für die Probenvorbereitung und unterstützt anspruchsvolle Anwendungen wie Verunreinigungsprofile oder pharmakokinetische Studien.
Detektoren wie Fluoreszenzdetektoren (FLD), elektrochemische Detektoren (ECD) und Massenspektrometrie (MS) erreichen extrem hohe Empfindlichkeiten – allerdings meist nur für bestimmte Substanzklassen.
2. Gute Selektivität oder Breite Anwendbarkeit – Wissen, was man misst
Die Selektivität beschreibt, wie gezielt ein Detektor auf einen Analyten reagiert, ohne durch Matrixbestandteile oder die mobile Phase beeinflusst zu werden.
Je nach Anwendung sollte ein Detektor entweder hochselektiv sein und nur Verbindungen mit bestimmten Eigenschaften erfassen (z. B. Fluoreszenz oder elektrochemische Aktivität), oder universell einsetzbar, um ein breites Spektrum an Substanzen unabhängig von ihrer Struktur zu detektieren.
3. Linearer Response und Großer Dynamischer Bereich – Den Zahlen vertrauen
Ein HPLC-Detektor sollte über einen möglichst großen Konzentrationsbereich hinweg eine lineare Response liefern. Das erlaubt die gleichzeitige Quantifizierung von Hauptkomponenten und Spurenverunreinigungen innerhalb eines Laufs. Ein großer dynamischer Bereich vereinfacht die Kalibrierung und erhöht die Zuverlässigkeit der Ergebnisse. Ebenso wichtig ist eine hohe Reproduzierbarkeit der Detektorsignale von Lauf zu Lauf.
4. Kompatibilität mit HPLC-Bedingungen – Problemloses Arbeiten mit der Methode
Ein idealer Detektor sollte problemlos mit isokratischen und Gradientenelutionen, gängigen mobilen Phasen und Additiven, sowie typischen Flussraten und Temperaturen kompatibel sein. Eine eingeschränkte Kompatibilität kann die Methodenentwicklung deutlich limitieren oder Kompromisse bei der Trennleistung erforderlich machen. Manche Detektoren liefern exzellente Ergebnisse – allerdings nur unter sehr spezifischen Bedingungen.
5. Stabilität und Geringes Rauschen – Signale klar erkennen
Eine stabile Basislinie mit geringem Rauschen und minimalem Drift verbessert das Signal-Rausch-Verhältnis und damit die Datenqualität erheblich. Dies ist besonders wichtig bei langen Messungen, Gradientenmethoden und Spurenanalysen.
6. Robustheit, Bedienkomfort und Wartungsaufwand – Unterstützung der täglichen Laborarbeit
Ein idealer Detektor sollte robust und über lange Messsequenzen hinweg zuverlässig arbeiten, sowie einfach einzurichten und zu bedienen sein und nur einen minimalen Wartungsaufwand benötigen. Für den Routinebetrieb im Labor sind Robustheit und Bedienkomfort in der Regel genauso wichtig wie die Leistung. Wartungsfreundlichkeit und unkomplizierte Fehlerbehebung sind wichtige Vorteile für Hochdurchsatzlabore. Aus praktischer und finanzieller Sicht sollte ein idealer Detektor auch geringe Wartungs- und Betriebskosten verursachen.
Die Realität: Man kann nicht alles haben
Da kein Detektor alle genannten Eigenschaften perfekt erfüllt, ist die Detektorauswahl immer ein Kompromiss zwischen Empfindlichkeit, Selektivität, Universalität, Robustheit und Kosten. Aus diesem Grund werden Multi-Detektor-Systeme (z. B. UV + CAD oder UV + MS) in modernen HPLC-Systemen immer häufiger eingesetzt, um die Stärken verschiedener Detektionsprinzipien zu kombinieren.
Tabelle 1: Übersicht über gängige Detektorklassen in der HPLC: Direkter Vergleich. (Grafik von KNAUER)
Kritische Leistungsparameter von HPLC-Detektoren
Datenaufnahmerate (Sampling Rate)
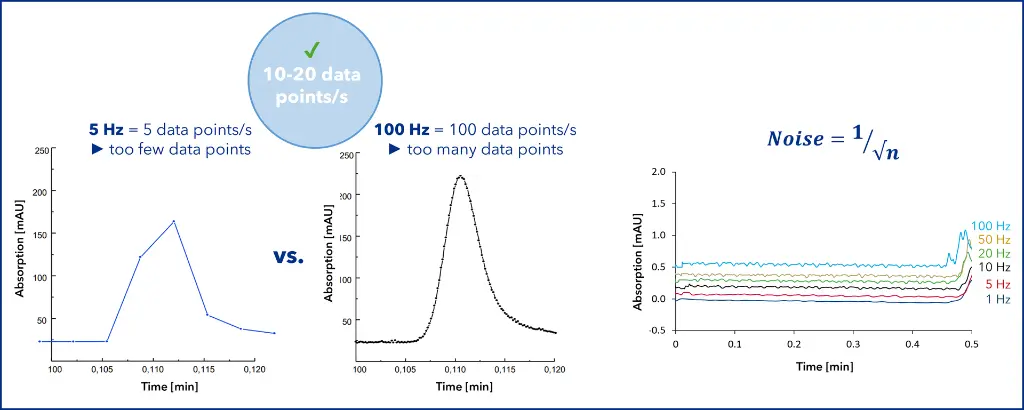
Abbildung 2: Beispiel für eine zu niedrige und zu hohe Datenaufnahmerate. (Grafik von KNAUER)
Die Datenaufnahmerate gehört zu den wichtigsten Einstellparametern eines Detektors. Sie beschreibt die Anzahl der Datenpunkte, die pro Sekunde erfasst werden, und beeinflusst Peakform, Reproduzierbarkeit, Flächenpräzision und Basislinienrauschen.
Je größer die Zahl, desto mehr Datenpunkte werden erfasst. Die erfassten Datenpunkte werden über einen definierten Zeitraum gemittelt und daraus das Chromatogramm aufgebaut.
Bei einer Datenrate von 5 Hz werden 5 Datenpunkte pro Sekunde aufgezeichnet. Wenn jedoch nicht genügend Datenpunkte vorhanden sind, erhält man eine unsaubere Peakdarstellung und unzuverlässige Ergebnisse (siehe Abbildung 2, links). Wenn der Wert auf 100 Hz eingestellt ist, werden 100 Datenpunkte pro Sekunde gesammelt, was in der Regel unnötig ist (Abbildung 2, Mitte). Die optimale Sampling Rate hängt von der Peakbreite ab. Für die meisten HPLC-Anwendungen liefern 10 bis 20 Hz eine glatte, symmetrische (gaussförmige) Peakform.
Ein Nebeneffekt hoher Datenaufnahmerate ist ein erhöhtes Basislinienrauschen, da das Rauschen statistisch mit 1/√n (n = Anzahl der Datenpunkte) definiert wird.
Rauschen und Drift
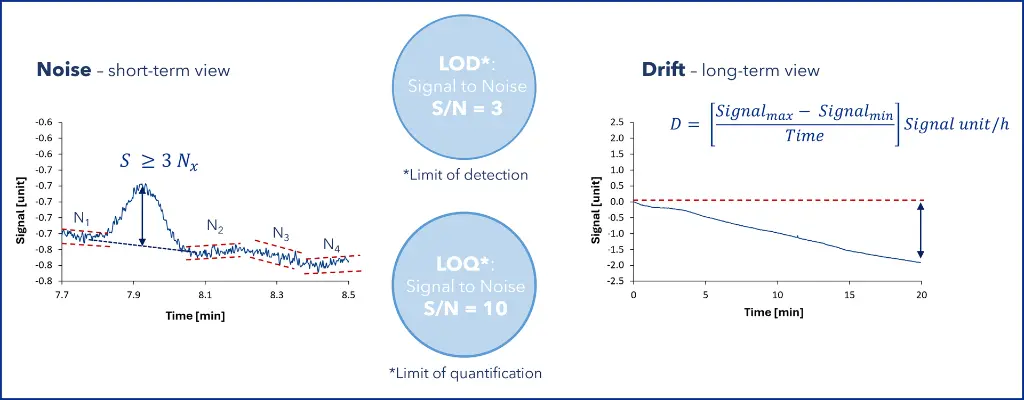
Abbildung 3: Basislinienrauschen und Drift. (Grafik von KNAUER)
Aber was genau ist eigentlich das Basislinienrauschen? Im Grunde genommen handelt es sich dabei um die Amplitude der Detektorbasislinie, ausgedrückt in geeigneten Detektoreinheiten, die alle Schwankungen innerhalb eines bestimmten Zeitfensters umfasst. Das Basislinienrauschen wird üblicherweise von Peak zu Peak einer Detektorbasislinie berechnet, die mit der verwendeten mobilen Phase gemessen wird.
Jeder HPLC-Detektor weist ein gewisses Maß an Rauschen auf, das unter anderem durch elektronisches Rauschen, Detektorzellenrauschen, Detektorinstabilität, Temperaturschwankungen und andere Einflüsse verursacht wird. Der Rauschpegel begrenzt wesentlich die Empfindlichkeit des Detektors, da Rauschen sich direkt auf das Signal-Rausch-Verhältnis (engl. signal-to-noise ratio (S/N)) auswirkt.
Ein Analyt-Peak kann zuverlässig identifiziert werden, wenn seine Höhe mindestens dreimal so hoch ist wie das berechnete Rauschen Dieser Parameter wird als Nachweisgrenze (engl. Limit of detection, LOD) bezeichnet. Die Quantifizierungsgrenze (engl. Limit of quantification, LOQ) einer Komponente muss höher sein und ist definiert als das Zehnfache des berechneten Rauschens.
Ein weiterer wichtiger Detektorparameter, der die Empfindlichkeit beeinflusst, ist der Drift der Detektor-Basislinie. Grundsätzlich ist der Drift eines Detektors über die Zeit ein guter Indikator für seine Langzeitstabilität. Es ist sinnvoll, das kurzfristige Rauschen von Peak zu Peak und den langfristigen Basislinien-Drift über ein bestimmtes Zeitfenster zu überprüfen. Der Drift ist die durchschnittliche Steigung/Änderung der Basislinie in der entsprechenden Zeiteinheit.
Starke Schwankungen des Basislinien-Drifts können ebenfalls die Empfindlichkeit beeinflussen und die Peak-Integration deutlich erschweren. Kurzzeitiges Basislinienrauschen wird häufig durch Verunreinigungen und Verschleiß/Alterung des Detektors beeinflusst. Langfristige Basislinien-Drift steht im Zusammenhang mit der Temperaturstabilität des Detektors und Äquilibrierungsprozessen.
Wie wählt man den richtigen HPLC-Detektor aus
Es gibt keinen „besten“ Detektor, nur den richtigen für die jeweilige Aufgabe. Hilfreiche Leitfragen sind:
1. Absorbiert mein Analyt UV-Licht oder fluoresziert er?
Wenn ja, sind optische Detektoren wie UV/VIS oder FLD oft die einfachsten und effektivsten Lösungen.
2. Hat mein Analyt keine Chromophore?
Wenn das der Fall ist, dann sind RID, ELSD oder CAD möglicherweise die besten Optionen.
3. Benötige ich Strukturinformationen?
Wenn ja, ist Massenspektrometrie hier die erste Wahl.
4. Ist extrem hohe Empfindlichkeit erforderlich?
Hierfür bieten die elektrochemische Detektion oder MS die besten Ergebnisse.
5. Analysiere ich Makromoleküle wie Polymere oder Proteine?
Hier liefern MALS und Viskosimetrie absolute Informationen zu Molekulargewicht, Größe und Verzweigung, unabhängig vom Elutionsverhalten.
Für eine vertiefende Entscheidungshilfe empfehlen wir unseren Blog “The way you look at it - A comprehensive guide for selecting the appropriate HPLC detector”. Treffen Sie Ihre Auswahl anhand dieser Faktoren, um optimale Ergebnisse bei Ihrer HPLC-Analyse zu erzielen.
Fazit
Das Verständnis der idealen Eigenschaften eines HPLC-Detektors erklärt, warum bestimmte Detektoren in speziellen Anwendungen besonders gut funktionieren und warum Kompromisse unvermeidlich sind. Gleichzeitig bietet es eine solide Grundlage für eine fundierte Detektorauswahl.
In den nächsten Beiträgen dieser Blogserie gehen wir detailliert auf die einzelnen HPLC-Detektionsprinzipien ein, beginnend mit der am häufigsten eingesetzten optischen Methode: der UV/VIS-Detektion.
Weitere Informationen zu diesem Thema erhalten Sie bei unserer Autorin: huhmann@knauer.net
Literatur
L. R. Snyder, J. J. Kirkland, J. W. Dolan, Introduction to Modern Liquid Chromatography, 3rd Edition, John Wiley & Sons, Inc., Hoboken, New Jersey, 2010.
D. A. Skoog, F. J. Holler, S. R. Crouch, Principles of Instrumental Analysis, 7th Edition, Cengage Learning, Boston, 2018.
R. P. W. Scott, Liquid Chromatography Detectors. In J. Chromatogr. Library, Vol. 11, Elsevier Scientific Publishing Company, Amsterdam, 1977, pp. iii-ix, 1-248.
V. R. Meyer, Praxis der Hochleistungs-Flüssigchromatographie, 10., vollst. überarb. u. erw. Auflage, Wiley-VCH, Weinheim, 2009.
G. Aced, H. J. Möckel, Liquidchromatographie, Apparative, theoretische und methodische Grundlagen der HPLC, VCH Verlagsgesellschaft mbH, Weinheim, 1991.

