
Science with Passion
App-Nr.: VBS0085
Version 1 03/2025
Einfaches und zuverlässiges Fraktionieren für Polysom-Profiling
U. Krop1, T.B.N. Ly-Hartig2, N. Muthukumarana2; krop@knauer.net
1KNAUER Wissenschaftliche Geräte GmbH, Hegauer Weg 38,
2Medizinische Fakultät Mannheim, Mannheim Institute for Innate Immunoscience (MI3), Franz-Volhard-Straße 6, 68167 Mannheim;
Illustration: Adobe Firefly
Zusammenfassung
Die Proteinsynthese ist ein entscheidender Prozess für alle lebenden Organismen. Schlüssel zu diesem Prozess ist die Translation von mRNA in Protein, die auf Ribosomen im Zytoplasma stattfindet. Um die Proteinsynthese zu beschleunigen, binden mehrere Ribosomen an das mRNA-Molekül, um ein Polysom zu bilden. Die Profilierung von Polysomen liefert daher wertvolle Informationen über die translationalen Aktivitäten der Zelle. Während des Profilierungsprotokolls werden mRNA, Ribosomen und Polysomen durch Sukrosegradientenzentrifugation getrennt und anschließend für die weitere Analyse fraktioniert. Hier beschreiben wir ein Standard-FPLC-System für die zuverlässige Fraktionierung von Polysomen. Das System umfasst eine faseroptische Flusszelle, um eine Peakverbreiterung zu verhindern, und nutzt das Leitfähigkeitssignal für einen optimierten Fraktionierungsstart. Dieser Ansatz optimiert die Fraktionierung von Polysomen.
Einführung
In den letzten Jahren gab es ein großes Interesse an der Rolle der translationalen Regulation der Genexpression in Organismen. Während der Translation wird die Nukleotidsequenz einer messenger RNA (mRNA) in die Aminosäuresequenz eines Proteins übersetzt. Ribosomen, die makromolekulare Komplexe sind, die in Zellen vorkommen, sind für die Proteinsynthese unerlässlich [1].
Ribosomen zeichnen sich durch ihren Sedimentationskoeffizienten S (Svedberg) aus. In eukaryotischen Zellen bestehen Ribosomen aus einer kleinen 40S-Untereinheit und einer großen 60S-Untereinheit, die insgesamt ein 80S-Ribosom bilden. Die Untereinheiten bestehen aus mehreren Proteinen und ribosomaler RNA (rRNA). Die prominenteste rRNA in der großen 60S-Untereinheit ist die 28S rRNA, während in der 40S-Untereinheit die 18S rRNA vorkommt. Diese rRNAs sind charakteristisch für die spezifischen Untereinheiten. Zusammen bilden die Komponenten das translational Apparatus. Die Effizienz der Translation wird durch die Bildung von Polysomen erhöht. Ein Polysom ist eine Gruppe von Ribosomen, die an ein mRNA-Molekül gebunden sind und linear angeordnet sind. Sie wurden erstmals in den 1960er Jahren von Wettstein et al. beschrieben, wobei ihre bedeutende Rolle bei der Proteinsynthese hervorgehoben wurde, und sie wurden zunächst als "Ergosomen" bezeichnet [2].
Die Polysom-Profilierung wurde entwickelt, um den translationalen Status einer spezifischen mRNA-Spezies zu untersuchen oder das Translatom zu analysieren, die Teilmenge von mRNAs, die in einer Zelle aktiv translatiert werden. Dies bietet wertvolle Einblicke in die translationalen Aktivitäten der Zelle. Die mRNA wird je nach Anzahl der gebundenen Ribosomen mithilfe eines Saccharosegradienten getrennt, was die Trennung von freier mRNA, ungebundenen 40S- und 60S-Untereinheiten, 80S-Monosomen und aktiv translatierten mRNAs, die von zwei oder mehr Ribosomen gebunden sind, ermöglicht. Sie kann mit globalen Analysetools wie DNA-Mikroarrays oder Hochdurchsatz-RNA-Sequenzierung kombiniert werden, um die RNA zu identifizieren [3, 4]. Hier beschreiben wir die Fraktionierung von Polysomen unter Verwendung eines speziellen FPLC-Systems.
Workflow für Polysom-Profiling und Probenvorbereitung
Die Probenvorbereitung wurde wie zuvor von Hoert et al. [4] beschrieben durchgeführt. Eine Übersicht über den Arbeitsablauf ist in Abbildung 1 dargestellt. Kurz gesagt, wurden Zelllysate aus kultivierten HCT 116-Zellen hergestellt. Die Lysate, die freie mRNA, Ribosomen und Polysomen enthielten, wurden dann durch Sukrose-Dichtegradienten-Zentrifugation (17,5–50%) getrennt. Nach der Zentrifugation wurde das Gradientenglas in den siFractor eingespannt und mit dem AZURA® FPLC-System verbunden. Der Boden des Glases wurde durchstochen, und der Gradient wurde mit einer 60%igen Sukroselösung verdrängt. Die Fraktionierung wurde durch das Leitfähigkeitssignal ausgelöst. Die gesammelten Fraktionen wurden durch denaturierende Gelelektrophorese analysiert. Eine anschließende Analyse der Fraktionen mit anderen Techniken ist ebenfalls möglich.
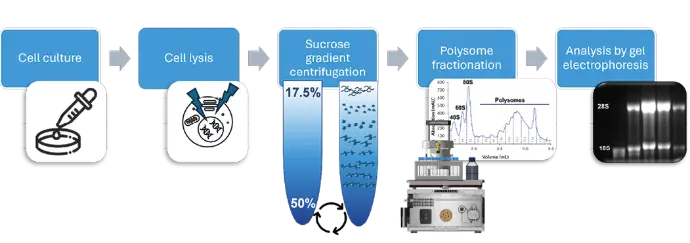
Abb. 1 Beispielhafter Arbeitsablauf für Polysomen-Profiling
Ergebnisse
Die Polysomen wurden mit einer FPLC und einer isokratischen Pumpe fraktioniert (Abbildung 2). Das Rohr, das den Saccharosegradienten enthält, wird mit dem siFractor-Gerät (nicht gezeigt) zwischen dem Mehrfachinjektionsventil und der Flusszelle des UV-Detektors platziert. Der Saccharosegradient wird von oben nach unten analysiert, indem der Gradient mit einer 60%igen Saccharoselösung verdrängt wird. Die Saccharoselösung, die verwendet wird, um den gebildeten Gradient zu bewegen, kann entweder aus einer variablen Proben-Schleife (z. B. Superloop) oder direkt von der Systempumpe gepumpt werden. Die Verwendung einer variablen Proben-Schleife vermeidet den Kontakt zwischen der Systempumpe und der Saccharoselösung, ist jedoch komplexer einzurichten und erfordert zusätzliche Schritte, um die Schleife zu füllen. Im gezeigten Fall wurde die 60%ige Saccharoselösung direkt durch die Pumpe gepumpt. Um die Bildung von Zuckerkristallen zu verhindern, wurde ein umfangreiches Pumpenspülverfahren in die Abschaltprozedur des Systems integriert. Der UV-Detektor ist mit einer Faseroptik-Flusszelle ausgestattet, die es ermöglicht, die Flusszelle direkt am Ausgang des Gradientrohrs zu platzieren, wodurch unnötiges Totvolumen und Peak-Breiterung eliminiert werden. Um die Reproduzierbarkeit der gesammelten Fraktionen zu erhöhen, wurde das Leitfähigkeitssignal verwendet, um die Fraktionierung auszulösen.
Abbildung 3 zeigt ein repräsentatives Chromatogramm für die Polysomfraktionierung. Freie mRNAs und tRNAs eluieren zuerst, gefolgt von den kleinen ribosomalen Untereinheiten (40S), den großen ribosomalen Untereinheiten (60S) und Monosomen (80S). Zwischen 2,5 und 4,5 ml eluieren die Polysomen aus dem Gradient. Jeder Peak entspricht einer spezifischen Anzahl von Ribosomen, die an mRNA gebunden sind.
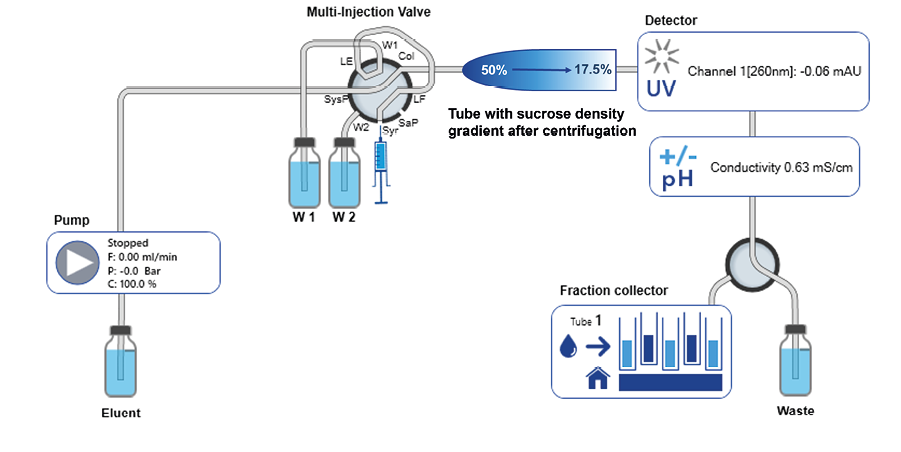
Abb. 2 FPLC-Systemflussweg und Verbindung des in den siFractor geklemmten Gradientenschlauchs
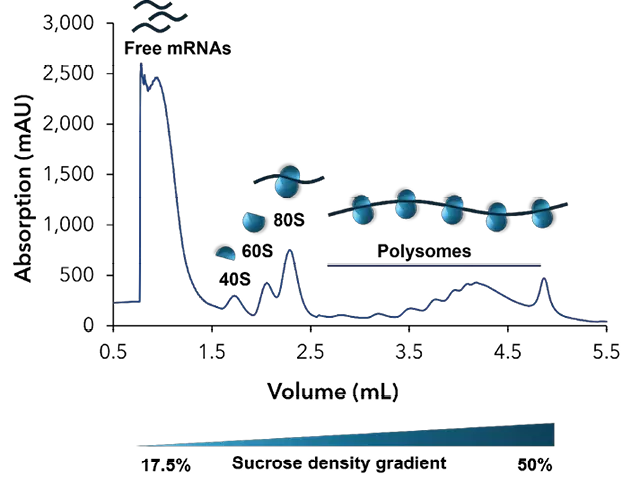
Abb. 3 Repräsentatives Chromatogramm des Saccharose-Gradientenprofils
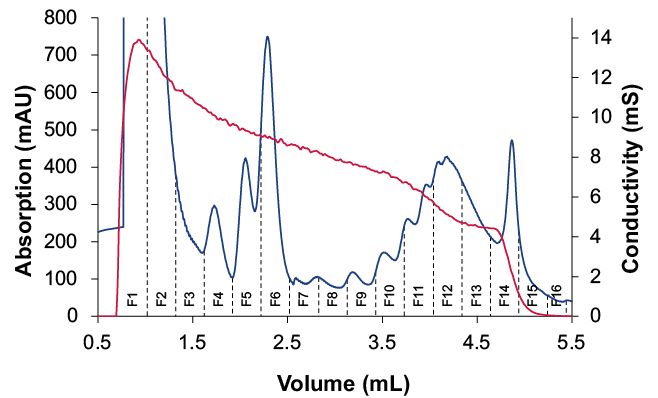
Eine detailliertere Ansicht der Polysomfraktionen ist in Abbildung 4A dargestellt. Das Leitfähigkeitssignal entspricht dem Beginn des Saccharosegradienten und wurde als Schwellenwert verwendet, um die Fraktionierung zu starten. Die gesammelten Fraktionen wurden durch Gelelektrophorese analysiert (Abb. 4B).
(A)
(B)
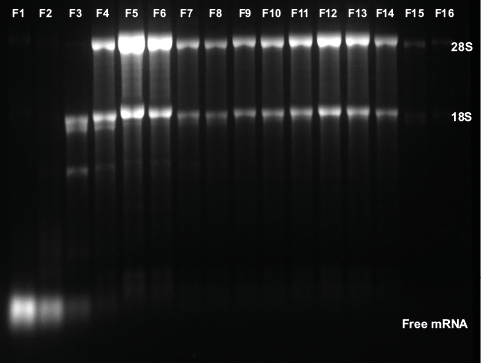
Abb. 4 Fraktionierung für Polysom-Profiling. (A) Vergrößerung des Chromatogramms des Saccharosegradienten und gesammelter Fraktionen, UV-Spur (blau), Leitfähigkeit (rot), Schwellenwert von 1 mS/cm wurde als Auslöser für den Beginn der Fraktionierung verwendet (B) Analyse der Fraktion durch Gelelektrophorese
Die großen Peaks repräsentieren freie mRNAs und tRNAs. Die kleine 40S-Untereinheit entspricht der 18S rRNA, und die 28S rRNA findet sich in den großen 60S-Untereinheiten. Folglich enthalten die Ribosomen- und Polysomenfraktionen 18S- und 28S-mRNA.
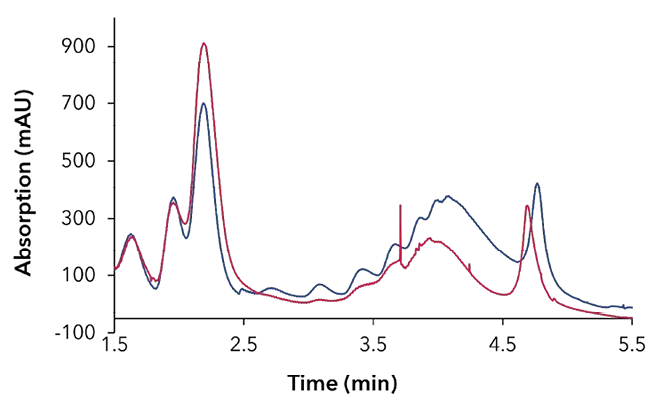
Die Polysom-Profilierung kann verwendet werden, um die translationalen Aktivitäten der Zelle zu analysieren. Ein Beispieldatensatz ist in Abbildung 5 dargestellt. Hier zeigt ein Vergleich von Kontroll- und mit Inhibitor behandelten Zellen eine deutliche Reduktion der Polysomen (Abb. 5 A), was auch durch die reduzierte Menge an 18S bestätigt wird.
und 28S-mRNA in den polysomalen Fraktionen (Abb. 5 B). Durch die Verwendung des Leitfähigkeitssignals als Schwellenwert zur Auslösung der Probenentnahme wird der Ausgangspunkt der Fraktionierung standardisiert, und die Fraktionen können genauer verglichen werden.
(A)
(B)
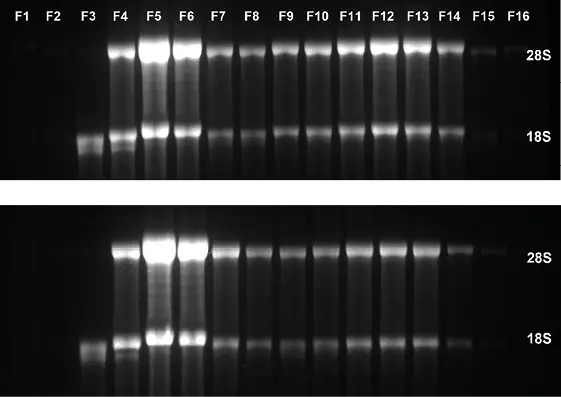
Abb. 5 Polysom-Profiling (A) Chromatogramm des Saccharosegradienten (blau) DMSO-behandelte Kontrollzellen, (rot) Zellen, die mit einem Inhibitor behandelt wurden, (B) Analyse der Fraktionen durch Gelelektrophorese (oben) DMSO-behandelte Kontrollzellen (unten) Zellen, die mit einem Inhibitor behandelt wurden
Fazit
Die Polysom-Profilierung ist eine bekannte Technik zur Analyse des Übersetzungsstatus von Zellen. Hier wird ein einfaches und praktisches FPLC-System beschrieben, das eine optimierte Fraktionierung von Ribosomen und Polysomen nach Sukrosegradientenzentrifugation ermöglicht. Durch die Verwendung des Leitfähigkeitssignals als Schwellenwert zur Auslösung der Probenentnahme wird der Ausgangspunkt der Fraktionierung standardisiert, und die Fraktionen können effizienter verglichen werden. Darüber hinaus reduziert die Verwendung einer faseroptischen Flusszelle das Totvolumen und verhindert eine Spitzenverbreiterung. Die Fraktionierung von Polysomen und Ribosomen mit dem optimierten AZURA FPLC ist zuverlässig, praktisch und ermöglicht eine anschließende Analyse der Fraktionen durch Gelelektrophorese oder zusätzliche Analysen zur Polysom-Profilierung.
Material und Methoden
Tab. 1 FPLC-Systemkonfiguration
Instrument | Beschreibung | Article No. |
ASM 2.2L | AZURA® Assistant ASM 2.2L Basiseinheit | |
P4.1S Pumpe | Kompakte Pumpe mit Drucksensor, | |
V4.1 Ventilantrieb | Universeller Ventilantrieb für ASM 2.2L | |
Multi-Injektionsventil | Multi-Injektionsventil, biokompatibel | |
UVD 2.1S-Faseroptikdetektor | Komakter variabler Einzelwellen-UV-Detektor mit Faseroptik für ASM 2.2L | |
UV-Flusszelle | Semi-präparative biokompatible 3 mm UV-Flusszelle, 1/16" Faseroptik-Version | |
Leitfähigkeitsmonitor | Leitfähigkeitsmonitor mikron 81 mit biokompatibler Durchflusszelle | |
FC 6.1 | Fraktionensammler | AFA00 |
Regal | Ständer für 165 Röhrchen 1/1,5/2 ml (11 mm) für | AFR01 |
SiFractor | Gerät zur Fraktionierung von Proben, die in Polypropylenröhren enthalten sind, die in Zentrifugationsanwendungen verwendet werden | n.a. |

Abb. 6 FPLC-Systemkonfiguration
Tab. 1 FPLC-Methodeneinstellungen
Parameter | Beschreibung |
Verschiebungslösung | 60% Saccharose |
Durchflussrate | 1 ml/min |
Ausführungszeit | 6 min |
Temperatur | Umgebung |
Erkennung | UV 260 nm, Leitfähigkeitsmonitor |
Datenrate | 10 Hz |
Fraktionierung |
|
Referenzen
[1] Alberts B, Johnson A, Lewis J, et al. Molekulare Biologie der Zelle. 4. Auflage. New York: Garland Science; 2002. Von RNA zu Protein. Verfügbar unter: https://www.ncbi.nlm.nih.gov/books/NBK26829/
[2] Wettstein Fo, Staehelin T, Noll H. Ribosomales Aggregat, das an der Proteinsynthese beteiligt ist: Charakterisierung des Ergosomes. Nature. 2. Februar 1963;197:430-5. doi: 10.1038/197430a0. PMID: 14000153.
[3] Shaffer D, Rollins JA. Fluoreszente Polysom-Profilierung in Caenorhabditis elegans. Bio Protoc. 2020 Sep 5;10(17):e3742. doi: 10.21769/BioProtoc.3742. PMID: 33659402; PMCID: PMC7842706.
[4] Hoerth K, Reitter S, Schott J. Normalisierte Ribo-Seq zur Quantifizierung absoluter globaler und spezifischer Veränderungen in der Translation. Bio Protoc. 20. Februar 2022;12(4):e4323. doi: 10.21769/BioProtoc.4323. PMID: 35340296; PMCID: PMC8899559.
Anwendungsdetails
Methoden | FPLC |
Modus | Andere |
Substanzen | Ribosomen, Zelllysate |
CAS-Nummer | # |


